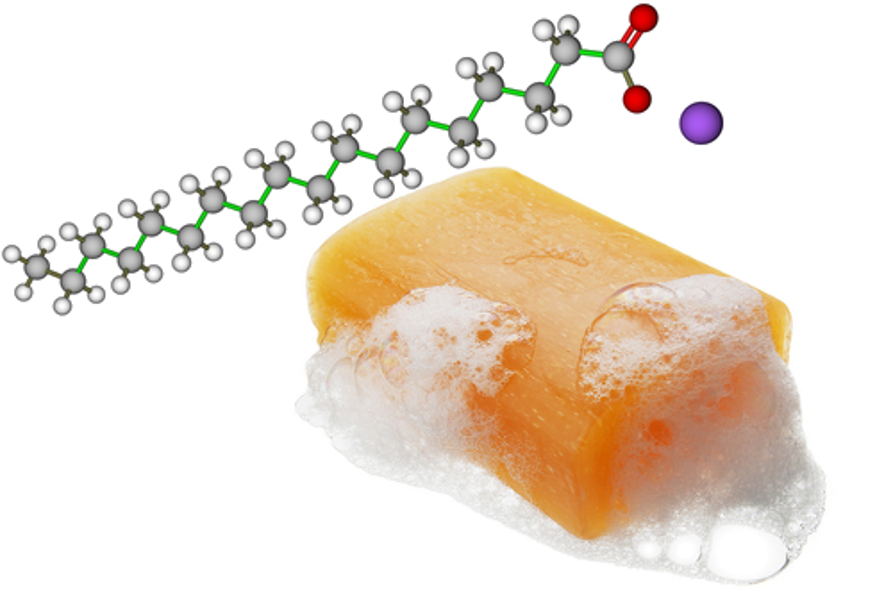
O sabão é constituído de um sal derivado de ácidos carboxílicos. Os sais de ácido carboxílico caracterizam-se pela presença do ânion carboxilato, que é mostrado a seguir:
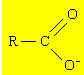
Ânion carboxilato - grupo funcional dos sais orgânicos derivados de ácidos carboxílicos
“R” é um radial alquila que, no caso dos sabões, é sempre uma cadeia bastante longa, em geral com 12 ou mais átomos de carbono.
A reação química que dá origem a esses sais de ácido carboxílico são reações de saponificação, que nada mais são do que uma hidrólise alcalina, ou seja, um triéster (triglicerídeo) reage com uma base em meio aquoso e forma um sal, que é o sabão, e um poliálcool.
Os triglicerídeos possuem longas cadeias porque eles são derivados de ácidos graxos, isto é, ácidos carboxílicos com mais de onze carbonos. Três ácidos carboxílicos reagem com o glicerol (glicerina) e originam o triglicerídeo, como mostrado a seguir:
.jpg)
Reação genérica de formação do triglicerídeo a partir de três ácidos graxos e uma glicerina
Em geral, os triglicerídeos são obtidos principalmente de óleos e gorduras. Assim, na reação de saponificação, coloca-se alguma gordura ou óleo para reagir com uma base, que geralmente é a soda cáustica (hidróxido de sódio, NaOH), em meio aquoso, formando um sal de ácido carboxílico, que é o nosso sabão, e o poliálcool, que é a glicerina:
.jpg)
Reação de saponificação para fabricação de sabão
Um exemplo de sabão obtido por esse método é o estereato de sódio (C17H35COO-Na+):
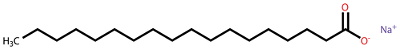
Fórmula do estereato de sódio, um sabão
Os sabões mais duros são os que possuem o sódio e são usados para limpeza comum. Para a obtenção de sabões mais moles, utiliza-se o hidróxido de potássio (KOH) no lugar do hidróxido de sódio (NaOH) na reação de saponificação. Os sabões de barra utilizam a gordura animal como matéria-prima, enquanto os sabonetes que usamos para a higiene pessoal são feitos com óleos vegetais no lugar da gordura.
Observe na composição química do sabão que suas moléculas sempre possuem uma cadeia carbônica bem longa, que é apolar, e uma extremidade polar. É por essa razão que os sabões conseguem limpar a gordura e a sujeira.
.jpg)
Estrutura típica de um sabão
O sabão funciona da seguinte maneira: a sua parte apolar é hidrofóbica, ou seja, tem aversão à água, mas é lipofílica, isto é, interage com as moléculas da gordura (que também são apolares), "aprisionando-as" dentro de uma micela, como mostra a imagem a seguir. Enquanto isso, as extremidades polares das moléculas do sabão, que são hidrofílicas, ficam voltadas para fora, interagindo com a água. Desse modo, a sujeira gordurosa é arrastada com a água.
Os sabões são também chamados de agentes tensoativos ou surfactantes(do inglês surface active agents = surfactants), pois eles diminuem a tensão superficial da água, ajudando a penetrar melhor nos materiais e a realizar a sua limpeza.
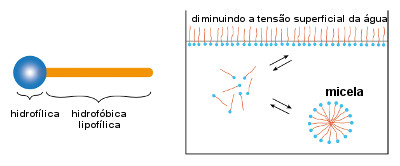
Ilustração de como o sabão funciona
A tensão superficial da água é aquela "película" que se forma em sua superfície em razão das ligações de hidrogênio entre suas moléculas. Alguns insetos, por exemplo, conseguem caminhar sobre as águas em razão dessa tensão superficial. Objetos leves, como um clipe, também ficam flutuando na superfície da água. Mas se a água estiver com sabão, essa tensão superficial é desfeita e o clipe afunda.
Por Jennifer Fogaça
Graduada em Química