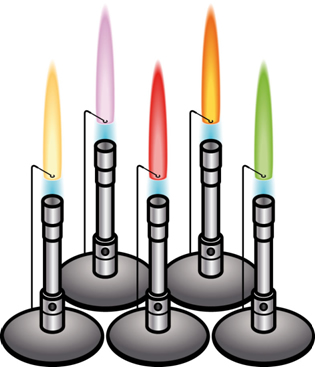
Quando submetemos diferentes sais inorgânicos à chama do bico de Bunsen observa-se a formação de chamas de cores diferentes. Por que isso acontece? Que sais podemos utilizar? Como realizar esse experimento?
Veja cada um desses aspectos a seguir:
Para realizar esse experimento você precisará de:
Materiais e reagentes:
-
Fonte de calor que tenha chama azul, de preferência um bico de Bunsen, mas pode ser também uma lamparina a álcool ou a chama de um fogão;

O teste de chama é feito com a chama azul do bico de Bunsen
-
Fósforos;
-
Fio de níquel-cromo (pode ser conseguido em lojas de materiais elétricos ou em arames de resistências de chuveiros. Se não conseguir, no texto será explicado outras formas em que se pode usar no lugar desse fio palitos de churrasco e algodão);
-
Pregador de roupas ou pinça de madeira (se for possível prender o fio de níquel-cromo);
-
Sais diversos, tais como sais de lítio, de cobre, de cálcio, de estrôncio e de sódio. Alguns exemplos de sais são: cloreto de lítio (LiCl), cloreto de bário (BaCl2), cloreto de sódio – sal de cozinha (NaCl), sulfato de cobre (CuSO4), cloreto de cálcio (CaCl2), cloreto de potássio (KCl) etc.;
.jpg)
Sais coloridos
-
Solução de ácido clorídrico a 1% em um béquer;
-
Esponja de aço;
-
Água destilada.
Procedimento experimental:
-
Antes de iniciar o experimento, limpe bem o fio de níquel-cromo com a esponja de aço e em água corrente. Depois de seco, prenda-o num cabo de madeira ou segure-o com o pregador;
-
Ligue o bico de Bunsen;
-
Faça uma pequena volta na ponta do fio de níquel-cromo e o mergulhe na solução de ácido clorídrico;
-
Pegue um pouco de um dos sais com a ponta do fio e coloque-a na chama;
-
Observe e anote o que aconteceu com a cor da chama;
-
Limpe o fio de níquel-cromo com a esponja de aço e água corrente;
-
Passe-o pelo ácido e repita o processo para todos os sais.
Outra forma de realizar esse processo é fazendo soluções de cada um dos sais. Depois se mergulha um palito de churrasco com algodão na ponta, que é, então, levado para a chama. Nesse caso, é importante trocar o algodão para cada solução de sal diferente.
Outra possibilidade é colocar cada uma dessas soluções em algum borrifador. Assim, é só borrifar a solução sobre a chama.
Resultados e Discussão:
A cor observada em cada chama é característica do elemento presente na substância aquecida. Por exemplo, ao se colocar o cloreto de sódio, sal de cozinha, na chama, a luz emitida é de um amarelo bem intenso, quando colocamos o sulfato de cobre, a luz emitida é de cor verde e o cloreto de cálcio emite uma luz vermelha.
Isso acontece porque cada elemento é formado por um átomo diferente, pois as suas camadas eletrônicas possuem valores de energia bem definidos, segundo o modelo atômico estabelecido por Böhr. Quanto mais distante do núcleo, maior é a energia do nível eletrônico.
Quando aquecemos o sal, ocorre o seguinte: o elétron absorve energia e salta para um nível mais externo, de maior energia. Dizemos que o elétron realizou um salto quântico e que está em um estado excitado. Porém, esse estado é instável e logo ele retorna para a sua órbita anterior, mas quando o elétron salta de um nível até outro que seja mais próximo do núcleo, ele libera energia. Essa liberação ocorre na forma de luz visível.
As cores são ondas eletromagnéticas, cada uma com um comprimento de onda diferente e que ficam na região do visível. Isso é demonstrado também quando o gás de algum elemento químico passa por um prisma e gera um espectro descontínuo, com raias ou bandas luminosas coloridas. Cada elemento apresenta um espectro diferente e constante.
Como os átomos de cada elemento possuem órbitas com níveis de energia diferentes, a luz liberada em cada caso será em um comprimento de onda também diferente, o que corresponde a cada cor.
Esse fenômeno foi empregado pelos chineses no século X para a criação dos fogos de artifício. Quando explodem, eles emitem uma luz de coloração branca, mas ao se acrescentar diferentes sais na sua composição, são obtidas as diversas cores que pintam os céus e fornecem um espetáculo maravilhoso.

Fogos de artifício coloridos
Por Jennifer Fogaça
Graduada em Química