A Eletrólise é um ramo estudado pela Eletroquímica, em que a energia elétrica é transformada em energia química, ou seja, trata-se de um processo inverso ao que ocorre nas pilhas. O processo das pilhas é espontâneo, mas o da eletrólise não é, pois é necessário que se forneça a corrente elétrica por meio de algum gerador, que pode até mesmo ser uma pilha ou bateria, para que uma reação de oxirredução aconteça.
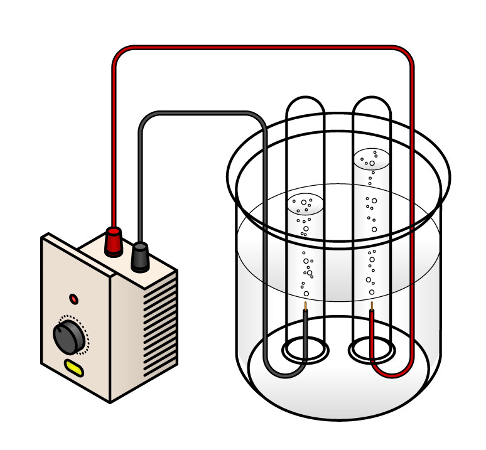
Toda eletrólise precisa do gerador de corrente contínua que passará a corrente elétrica por um líquido com íons, que é chamado de eletrólito. No eletrólito ficam imersos dois eletrodos, que geralmente são inertes, feitos de platina ou de grafita, sendo que um é o cátodo (polo negativo) e o outro é o ânodo (polo positivo). O recipiente onde fica o eletrólito e os eletrodos mergulhados nele, bem como onde ocorre todo o processo de oxirredução, é chamado de cuba eletrolítica.
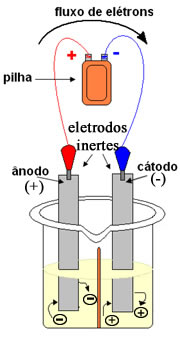
Cuba eletrolítica e outras partes de eletrólise
A eletrólise ocorre, então, da seguinte maneira: quando o gerador é ligado, os elétrons são transportados do gerador pelo seu polo negativo (no caso da pilha, o polo negativo é o ânodo) e entram na cuba eletrolítica pelo cátodo (polo negativo, no caso da eletrólise), onde acontece uma reação de redução, em que se recebem os elétrons, como mostra a semirreação genérica abaixo:
Cátodo (polo negativo): Redução: Cx+ + x e- → C
Então, na cuba eletrolítica, os elétrons emergem do ânodo (polo positivo na eletrólise), onde ocorre a oxidação, isto é, a perda de elétrons, e chegam ao gerador pelo seu polo positivo (cátodo). A semirreação de oxidação que ocorre no ânodo da célula eletrolítica é dada abaixo de forma genérica:
Ânodo (polo positivo): Oxidação: Ay-→ A + y e-
A reação global é dada pela soma dessas duas semirreações. Desse modo, a energia que foi usada para provocar a descarga dos íons, no final da reação, produz substâncias simples ou metálicas muito usadas nas indústrias. Tal energia é a energia elétrica que fica armazenada nessas substâncias na forma de energia química.
Dependendo do tipo de eletrólito, a eletrólise pode ser classificada de duas formas:
1. Eletrólise ígnea: O eletrólito é uma substância fundida, isto é, que está no estado líquido sem a presença de água, porque o ponto de fusão dos materiais derretidos geralmente é bem elevado.
Por exemplo, a eletrólise do sal de cozinha fundido (cloreto de sódio - NaC?) produz duas substâncias muito importantes e que não são encontradas de forma isolada na natureza, que são o sódio metálico (Na(s)) e o gás cloro (Cl2(g)). O ponto de fusão do sal é superior a 800,4 ºC, portanto, com toda certeza, não há água no meio, tendo em vista que o ponto de fusão da água é de 0º C e o de ebulição é de 100 ºC ao nível do mar.
Quando se passa a corrente elétrica pelo sal fundido, ocorrem as seguintes reações:
Cátodo: Na+(l) + e- → Na(s)
Ânodo: 2Cl-(l) → 2 e- + 1Cl2(g)____________
Reação Global: Na+(l) + 2Cl-(l) → Na(s) + 1Cl2(g)
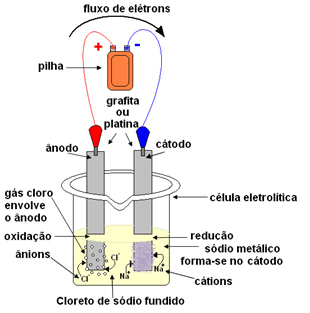
Esquema da eletrólise do cloreto de sódio fundido
2. Eletrólise em meio aquoso: Nesse caso, o eletrólito é uma solução aquosa com íons dissolvidos.
Na eletrólise em meio aquoso existem, além dos íons da substância dissolvida, os íons da água (H+ e OH-). Assim, é preciso consultar listas de facilidade de descarga para saber qual será o ânion e qual será o cátion que participarão das reações de oxirredução e ficarão neutros.
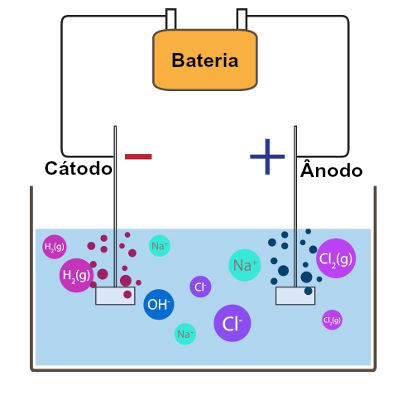
Por exemplo, no caso da eletrólise da salmoura (sal dissolvido na água), temos os quatro íons: Na+ e H+, Cl- e OH-. Consultando a fila de facilidade de descarga elétrica, vemos que o H+ tem maior facilidade que o Na+ e também notamos que o Cl- tem maior facilidade que o OH-. Assim, o cátion Na+ e o ânion OH-?permanecerão na solução (são os “íons espectadores”), enquanto o H+ e o Cl- irão reagir:
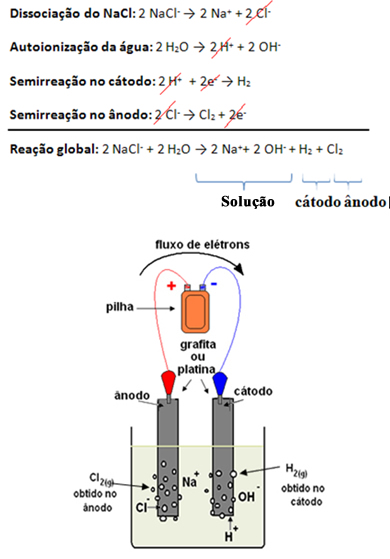
Reações envolvidas na eletrólise da salmoura
Por Jennifer Fogaça
Graduada em Química
Aproveite para conferir nossa videoaula relacionada ao assunto: