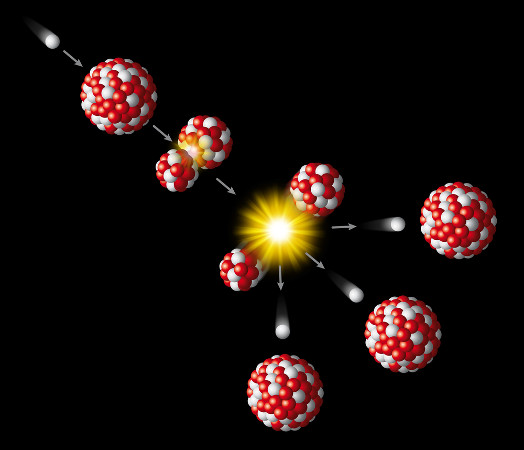
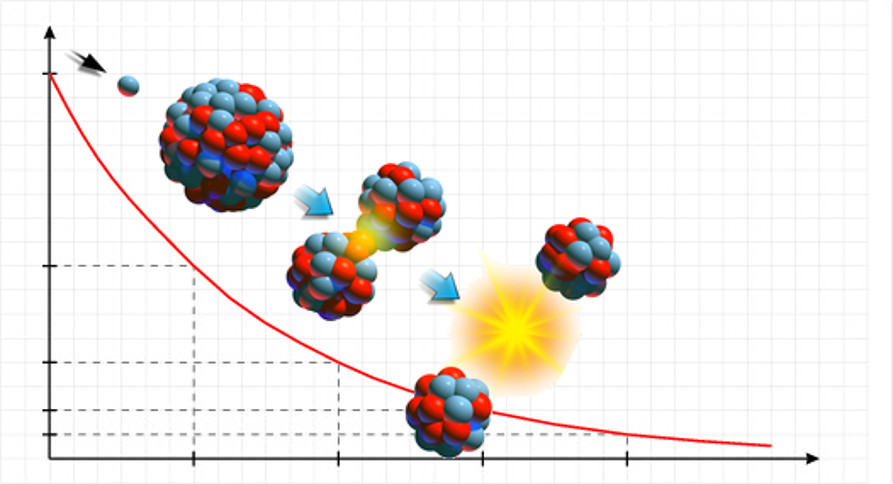
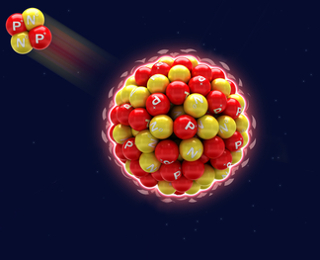
Em 1900, o físico neozelandês Ernest Rutherford (1871-1937) realizou um experimento no qual ele colocou uma amostra de polônio em um bloco de chumbo com apenas uma cavidade. O polônio é um material radioativo, assim, as suas radiações foram dirigidas por meio de duas placas carregadas eletricamente rumo a uma placa recoberta com sulfeto de zinco (ZnS), que é fluorescente e emite luminosidade quando atingido por radiações.
Ele observou o que é mostrado na figura abaixo, três emissões radioativas diferentes. Ele denominou de alfa (α) as emissões que eram positivas, pois se desviaram no sentido da placa negativa. As emissões negativas foram chamadas de beta (β), pois se desviaram no sentido da placa positiva. Além disso, o desvio da radiação beta era maior que o da radiação alfa. Enquanto isso, a terceira radiação, denominada de gama (γ), não sofreu desvio nenhum.
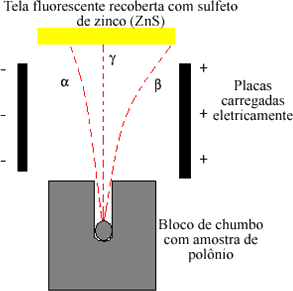
Esquema do experimento de Rutherford
Vejamos a constituição de cada uma dessas emissões radioativas naturais e, dessa forma, entenderemos porque Rutherford observou esse comportamento.
-
Emissões alfa (α):
Essa radiação é constituída de dois prótons e dois nêutrons, exatamente como o núcleo de um átomo de hélio. Visto que cada próton possui carga elétrica +1 e cada nêutron não possui carga, mas ambos possuem massa de 1 u, uma partícula alfa possui carga +2 e massa 4 u.
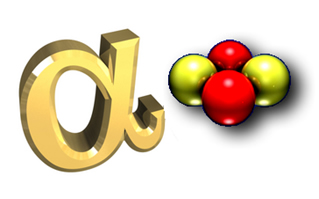
A emissão alfa é constituída de dois prótons e dois nêutrons
É por isso que essa emissão sofreu desvio no sentido da placa negativa, isto é, porque ela é carregada positivamente e possui massa.
A simbologia usada para qualquer átomo ou partícula subatômica é:
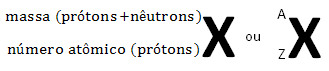
Simbologia usada em representação de átomos e partículas subatômicas
Desse modo, as partículas alfa podem ser representadas da seguinte forma:
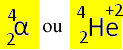
Representação de partícula alfa
Os elementos radioativos possuem um núcleo instável, assim, quando eles emitem uma partícula alfa, eles se transmutam em outro elemento com massa menor 4 unidades e número atômico menor 2 unidades. Veja um exemplo abaixo:
92235U → 90231Th + 24α
-
Emissão beta (β):
Essa radiação é constituída de partículas leves com carga elétrica negativa, semelhante a elétrons (carga igual a +1). Visto que a massa de um elétron é muito menor que a massa do próton ou a massa do nêutron, considera-se que a massa da partícula beta é desprezível. É por isso que o seu desvio é maior que o das partículas alfa.
As partículas betas podem ser representadas por:
![]()
Representação de partícula beta
Os núcleos instáveis tendem a se rearranjar para adquirir estabilidade, dessa forma, um ou mais de seus nêutrons sofrem uma transformação em 1 próton, 1 neutrino e 1 elétron. O próton permanece no núcleo, o neutrino e o elétron (partícula beta) são emitidos pelo núcleo.
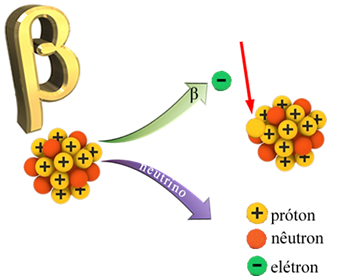
Emissão beta e de neutrino pelo núcleo
Assim, quando um elemento radioativo emite uma partícula beta, ele se transforma em um isóbaro, isto é, elemento com mesmo número de massa (pois ele perdeu um nêutron, mas ganhou um próton) e com número atômico (número de prótons) maior 1 unidade.
Exemplo: 614C → 714N + -10β
-
Emissão gama:
Ao contrário das anteriores, a radiação gama não se trata de uma partícula, mas sim de uma radiação eletromagnética semelhante aos raios X. Você pode ver essa radiação no espectro eletromagnético abaixo:
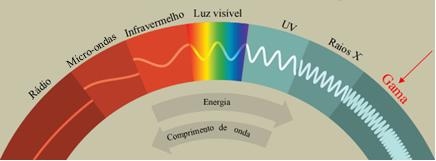
Espectro eletromagnético com radiação gama em destaque
Visto que se trata de uma onda eletromagnética, e não de uma partícula, a radiação gama não possui carga nem massa e, por isso, não sofreu desvio no experimento de Rutherford. Sua representaçaõ é dada simplesmente por: γ.

A emissão gama é uma onda eletromagnética
Dentre essas três emissões radioativas naturais, a radiação gama é a mais perigosa. Como não é uma partícula, ela não sofre interferência dos elétrons e prótons dos átomos do material e, por isso, tem um alto poder de penetração.
O poder de penetração das partículas α é pequeno, não atravessando sequer uma folha de papel, e, no corpo humano, elas são detidas pela camada de células mortas da pele. As partículas β têm um médio poder de penetração, atravessando uma folha, mas sendo detidas por 1 cm de uma chapa de alumínio. No ser humano, ela penetra até 2 cm e pode causar danos sérios.
Já as partículas gama atravessam 15 cm de aço e são detidas por placas de chumbo de 5 cm ou mais. Podem atravessar totalmente o corpo humano, causando danos irreparáveis.
* Crédito da imagem: IgorGolovniov / Shutterstock.com
Aproveite para conferir nossa videoaula relacionada ao assunto: