Na Termoquímica, estudam-se os processos físicos e as reações químicas que envolvem troca de calor, sendo que os processos endotérmicos são aqueles em que o calor é absorvido, enquanto os processos exotérmicos são os que liberam calor. Por exemplo, a combustão da madeira em uma fogueira libera energia na forma de calor e, portanto, é uma reação exotérmica.
Mas, então, surge uma pergunta: De onde surgiu essa energia que foi liberada?
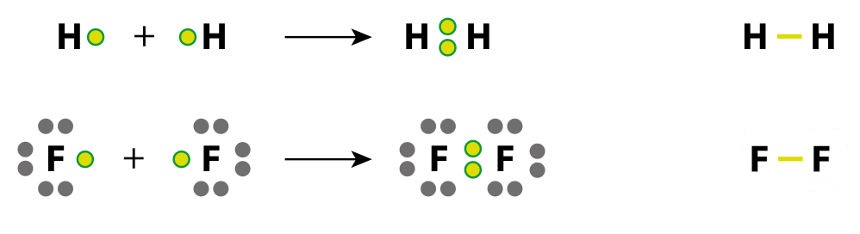
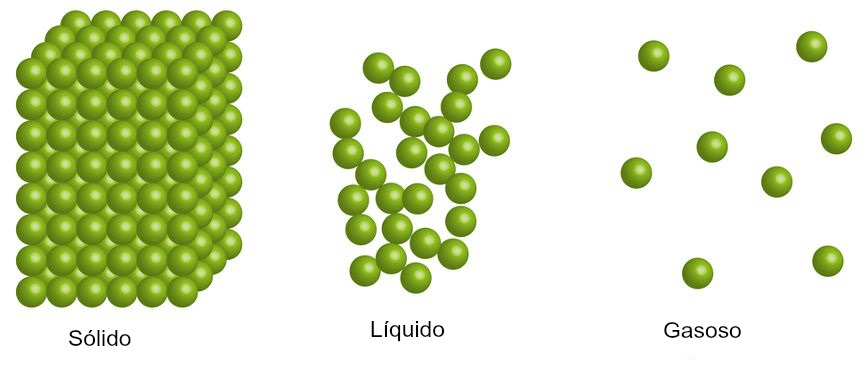
Na verdade, essa energia estava contida nos reagentes e, quando eles se transformaram nos produtos, ela foi liberada. A energia já existente nas moléculas é proveniente da sua movimentação, que no estado gasoso é caótica. Esse conteúdo específico de energia interna que cada substância possui é denominado de entalpia e é simbolizado por “H”.
No entanto, até o momento, não se sabe uma forma de determinar experimentalmente o valor exato da entalpia de cada um dos reagentes ou de cada um dos produtos. O que se costuma determinar é a variação da entalpia (ΔH) do processo. Para tal, usam-se calorímetros, que são aparelhos que medem a quantidade de calor liberada em uma reação.
A fórmula usada para calcular a variação da entalpia é:
ΔH = HFINAL – HINICIAL ou ΔH = HPRODUTOS – HREAGENTES
Se o valor der negativo, isso significa que a reação é exotérmica, pois foi liberado calor e o valor da entalpia dos produtos é menor que a entalpia dos reagentes. Por outro lado, se o valor de ΔH der positivo, a reação é endotérmica, pois com a absorção de energia, a entalpia dos produtos será maior que a dos reagentes.
-
ΔH < 0 → exotérmica;
-
ΔH > 0 → endotérmica.
Por exemplo, a queima do carvão libera 393 kJ de energia na forma de calor, assim o valor da variação da entalpia nessa reação é dado por: ΔH = -393 kJ.
C(s) + O2(g) → CO2(g) ΔH = -393 kJ
Já a reação de decomposição da água, mostrada abaixo, absorve calor e sua variação de entalpia é positiva:
H2O (Δ) → H2(g) + ½ O2(g) ΔH = +285,5 kJ
Outro ponto importante é que visto que o ΔH depende de uma série de fatores, tais como temperatura, pressão, estado físico e número de mol, criou-se um referencial para que se compare a entalpia da substância, que foi denominada entalpia padrão (H0), que considera a substância no seu estado mais estável, sob pressão de 1 atm e temperatura de 25ºC.
Quando todos os reagentes e produtos de uma reação estão no seu estado padrão, a variação de entalpia será denominada variação de entalpia padrão (ΔH0).
Existem vários tipos de entalpia, dependendo dos vários tipos de reações e mudanças de estado físico. Eles são:
- Entalpia de Mudança de Estado Físico: energia necessária para que 1 mol de substância, nas condições padrão de temperatura e pressão, mude de estado físico e inclui entalpia de vaporização, entalpia de fusão, entalpia de liquefação e entalpia de solidificação;
- Entalpia de Formação: calor liberado ou absorvido na formação de 1 mol de uma substância a partir de seus elementos constituintes, que são substâncias simples, no estado padrão, com a entalpia igual a zero;
- Entalpia de Combustão: energia liberada na combustão completa de 1 mol de uma substância no estado padrão;
- Entalpia de Neutralização: é a energia liberada na forma de calor, na reação entre 1 mol de H+(aq) e 1 mol de OH-(aq), fornecidos respectivamente por um ácido e uma base fortes, para a formação de 1 mol de água;
- Entalpia de Solução: é a soma da entalpia reticular (absorve energia) e da entalpia de hidratação (libera energia). Ocorre quando se dissolve um soluto na água, gerando uma solução.
Por Jennifer Fogaça
Graduada em Química
Videoaulas relacionadas: