O estudo cinético de uma reação química envolve o conhecimento da velocidade em que ela é processada. A Cinética Química, em razão do seu objetivo de estudar essa velocidade, é muito importante para o dia a dia da humanidade. As aplicações desse ramo da Química são muitas e ocorrem no ramo industrial, na prática agrícola e farmacêutica, entre outras.
Em casa, utilizamos conhecimentos cinéticos de reações químicas quando realizamos atividades simples, tais como:
-
Colocar alimentos diversos na geladeira;
-
Congelar carnes no freezer ou congelador;
-
Cortar batatas em pedaços menores para cozinhar;
-
Utilizar fermento ao fazer um bolo.
Observação: Os exemplos nos dão uma noção de como a Cinética Química é importante para o ser humano de forma geral.
Uma reação química deve apresentar obrigatoriamente dois grupos de substâncias, que são os reagentes (A e B) e os produtos (C e D), como na equação representada a seguir:
![]()
Equação que representa uma reação química qualquer
A velocidade de uma reação química qualquer pode ser calculada a partir de uma lei criada em 1864 por dois químicos, Cato Maximilian Guldberg e Peter Waage, ambos noruegueses, que realizaram um importante estudo experimental sobre os fatores que seriam determinantes na velocidade de uma reação.
Eles descobriram que, em uma reação química, a concentração dos reagentes, seus expoentes estequiométricos (números utilizados para balancear a equação) e a temperatura são fundamentais na determinação da velocidade de uma reação. A partir dessa constatação, criaram uma expressão matemática que representa a chamada Lei da ação das massas de Guldberg e Waage ou, simplesmente, Lei da velocidade:
v = K. [A]a.[B]b
Observação: A lei é enunciada com o termo ação das massas porque se refere à concentração em mol/L.
A seguir temos a especificação de cada um dos componentes da expressão da lei da velocidade:
-
v = velocidade da reação;
-
K = constante da velocidade, que depende exclusivamente da temperatura;
-
[A ou B] = concentração em mol/L de cada reagente;
-
a ou b = ordem de cada um dos reagentes (a ordem de um participante é a influência que ele exerce na velocidade da reação).
Como a lei da velocidade ou da ação das massas é feita de forma absolutamente experimental, quando vamos utilizá-la para determinar a velocidade de uma reação em um exercício, sempre utilizamos o tipo de reação fornecido. Quanto a esse fato, podemos ter dois tipos de reações:
a) Reação elementar
É a reação química que se processa em uma única etapa. Assim sendo, a ordem de cada um dos reagentes que serão utilizados no cálculo da velocidade da reação é o próprio coeficiente estequiométrico presente na equação. Por exemplo:
![]()
Equação da síntese da água
Nessa reação podemos observar que o coeficiente estequiométrico do N2 é 1 e do H2 é 2. Assim, o N2 é um reagente de 1a ordem e o H2 é um reagente de 2a ordem. A expressão da velocidade para essa reação química seria:
v = K. [H2]2.[O2]1
b) Reação não elementar
É uma reação química que se processa em mais de uma etapa, ou seja, para ocorrer, ela depende de outras reações para formá-la (reação global). Por exemplo:
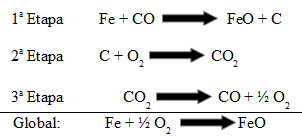
Equações químicas que envolvem a formação do óxido de ferro II (FeO)
Analisando o exemplo, podemos observar que a síntese do óxido de ferro II (reação global) envolve três outras etapas (três outras reações químicas). Cada uma dessas etapas ocorre com uma velocidade diferente uma da outra. De acordo com Guldberg e Waage, a etapa mais lenta é a que contribui diretamente para a determinação da velocidade da reação.
Quando temos uma reação não elementar para realizar o cálculo da velocidade, a ordem de cada um dos participantes será determinada por cálculos individuais, já que, nesses casos, trata-se de um dado absolutamente experimental. Essa determinação das ordens dos reagentes é feita por meio de uma tabela com valores fornecida pelos exercícios, já que são dados experimentais. A seguir temos um exemplo de tabela para a reação de síntese da amônia (reação global):
![]()
Equação da síntese da amônia
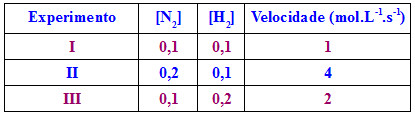
Na tabela podemos observar que há três experimentos (que representam etapas da reação), as concentrações dos reagentes e a velocidade de cada etapa.
Para determinar a ordem de cada um dos reagentes, já que é uma reação não elementar e não podemos utilizar os valores dos coeficientes da equação porque ela se processa em mais de uma etapa, vamos fazer um cálculo simples verificando o efeito da concentração na velocidade por meio das seguintes regras:
-
Escolher dois experimentos na tabela;
-
Se for determinar a ordem de um reagente, a concentração do outro reagente nos dois experimentos deverá ser a mesma;
-
Comparar o efeito da concentração do reagente do qual se quer descobrir a ordem com a velocidade.
Seguindo as regras acima, vamos determinar as ordens de N2 e H2:
♦ Para a ordem do N2:
-
serão escolhidos os experimentos I e II;
-
nesses experimentos, a concentração de N2 mudou e a do H2 não.
Comparando a concentração com a velocidade, temos que do experimento I para o experimento II, a concentração de N2 dobrou, enquanto a velocidade quadruplicou. Comparando:
[ ] = V
2 = 4
Se colocarmos ambos com a mesma base, teremos:
[ ] = V
2 = 22
Assim, temos que o que diferencia um do outro é o expoente 2 e, por isso, vamos considerar o reagente N2 de 2a ordem.
♦ Para a ordem do H2:
-
serão escolhidos os experimentos I e III;
-
neles, a concentração de H2 mudou e a do N2 não.
Comparando a concentração com a velocidade, temos que do experimento I para o experimento III, a concentração de H2 dobrou e a velocidade também. Comparando:
[ ] = V
2 = 2
Assim, como eles já apresentam a mesma base, consideramos o reagente H2 de 1a ordem. Com isso, a expressão da velocidade para esse exemplo seria:
v = K. [N2]2.[H2]1
Por Me. Diogo Lopes Dias
Aproveite para conferir nossa videoaula sobre o assunto:



