Sabemos, de uma forma geral, que existem várias transformações de estados físicos que podem acontecer com a matéria, sendo elas:
-
Fusão: Passagem do sólido para o líquido
-
Solidificação: Passagem do líquido para o sólido
-
Vaporização: Passagem do líquido para o gasoso
-
Condensação ou Liquefação: Passagem do gasoso para o líquido
-
Sublimação: Passagem do sólido para o gasoso
-
Ressublimação: Passagem do gasoso para o sólido
Essas transformações podem ocorrer através da modificação de uma ou duas variáveis, que são temperatura e pressão. Assim, dependendo das condições que a matéria estiver sendo submetida, se utilizarmos apenas a mudança na temperatura ou na pressão a mudança de estado irá ocorrer; caso contrário a mudança nas duas variáveis é necessária.
Para melhor visualizar a forma como temperatura e pressão estão diretamente relacionadas com as mudanças de estados físicos foi desenvolvido um diagrama, chamado de diagrama de fases, que nos mostra as variações que esses dois parâmetros podem sofrer e as transformações físicas que ocorrem. Podemos observar nele qual é a fase física mais estável de uma determinada substância em cada condição de temperatura e pressão. Abaixo temos uma representação geral de um diagrama de fases:
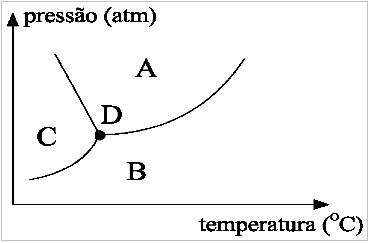
Diagrama de fases geral para a matéria
Podemos observar que ele apresenta a variável pressão no eixo x e a variável temperatura no eixo y. É composto de três regiões (A, B, C), três curvas (entre C e A, entre C e B, entre A e B) e um ponto central (D) que interliga as três curvas.
1- Estudo do diagrama de fases
Cada detalhe de um diagrama de fases está descrito logo a seguir:
a) Regiões
-
Região A: é a região que nos mostra quais são as condições de temperatura e pressão para que o estado líquido seja predominante (mais estável).
-
Região B: é a região que nos mostra quais são as condições de temperatura e pressão para que o estado vapor seja predominante (mais estável).
-
Região C: é a região que nos mostra quais são as condições de temperatura e pressão para que o estado sólido seja predominante (mais estável).
b) Curvas
-
entre C e A: essa curva é chamada de curva solidificação, na qual temos as condições de temperatura e pressão para que as fases sólida e líquida coexistam em equilíbrio. É zona limítrofe entre os estados sólido e líquido. Assim, qualquer ponto localizado sobre ela indica que teríamos a substância nos estados sólido e líquido.
-
entre C e B: essa curva é chamada de curva ressublimação, na qual temos as condições de temperatura e pressão para que as fases sólida e gasosa coexistam em equilíbrio. É zona limítrofe entre os estados sólido e vapor. Assim, qualquer ponto localizado sobre ela indica que teríamos a substância nos estados sólido e vapor.
-
entre A e B: essa curva é chamada de curva condensação, na qual temos as condições de temperatura e pressão para que as fases líquida e gasosa coexistam em equilíbrio. É zona limítrofe entre os estados líquido e vapor. Assim, qualquer ponto localizado sobre ela indica que teríamos a substância nos estados líquido e vapor.
c) Ponto Central (D)
Esse ponto é chamado de ponto triplo, já que nele temos uma condição de temperatura e uma condição de pressão na qual encontramos a substância nos três estados físicos da matéria (sólido, líquido e vapor) ao mesmo tempo.
2- O diagrama de fases da água e o grau de liberdade
Temos abaixo um exemplo de um diagrama de fases específico de uma substância, a água. Nele, podemos observar alguns detalhes que são muito importantes como as condições para a ocorrência do ponto triplo, as condições específicas de cada estado, o ponto crítico etc.
O ponto crítico (C) indica pra nós qual é a condição para que a divisória entre líquido e vapor desapareça, ou seja, a partir desse ponto teremos a substância no estado gasoso. Assim teremos uma única fase uniforme. No caso da água, isso ocorre a uma temperatura crítica (tc) de 374 oC e uma pressão de 218 atm. A partir desses valores de temperatura e pressão temos a água gasosa.
Outro detalhe que pode ser avaliado no diagrama de fases é o que chamamos de grau de liberdade. Denomina-se grau de liberdade o número de variáveis que podem ou não ser alteradas, sem que o número de fases físicas se altere. É importante dizer que o grau de liberdade depende da parte do diagrama que estivermos avaliando: curva, região ou ponto triplo.
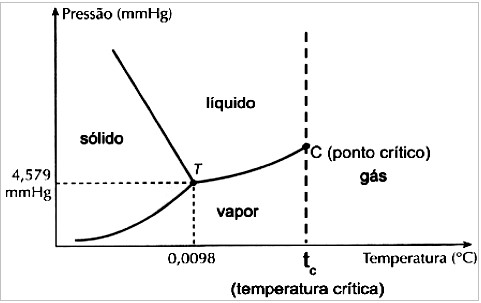
Diagrama de fases da água
Analisando o diagrama de fases da água podemos discutir bem a questão do grau de liberdade. Por exemplo:
-
Ponto T: No ponto T, que é o ponto triplo, temos um grau de liberdade igual a zero, pois não temos a liberdade de variar nem a temperatura nem a pressão.
-
Região Sólida: Se determinarmos um valor específico de temperatura (de baixo para cima, na vertical, teremos vários valores de pressão que determinariam esse estado. Se fizermos o inverso, determinando um valor fixo de pressão (da esquerda para a direita) o mesmo ocorreria com a temperatura. Por conta disso dizemos que o grau de liberdade é igual a 2.
-
Curva de solidificação: Nela podemos observar que se marcamos um ponto sobre a curva, esse ponto estará relacionado a um valor de pressão único e um valor de temperatura único. Assim, escolhida uma temperatura sobre um ponto da curva, automaticamente estaremos escolhendo o valor de pressão que corresponde àquela temperatura e vice-versa. Por conta disso dizemos que o grau de liberdade aqui é igual a 1.
Observação: Um físico norte americano chamado Josiah W. Gibbs desenvolveu uma fórmula na qual podemos determinar o grau de liberdade de uma substância em qualquer área do diagrama de Fases. Nela temos L, que é o grau de liberdade; C, que é o número de combinações de componentes; e F, que é o número de fases.
|
L = C + 2 – F |
Assim, se quisermos determinar o grau de liberdade sobre a curva de solidificação temos que:
C = 1 (escolher a temperatura, escolher a pressão automaticamente)
F = 2 (temos sólido e líquido)
L = 1 + 2 – 2
L = 1,
Por conta disso chamamos esse sistema de univariante, ou seja, possui apenas uma variável que pode ser escolhida.
Agora, escolha o ponto triplo ou um ponto qualquer de uma região do diagrama e determine o grau de liberdade. Bom estudo!
Por Me. Diogo Lopes Dias


