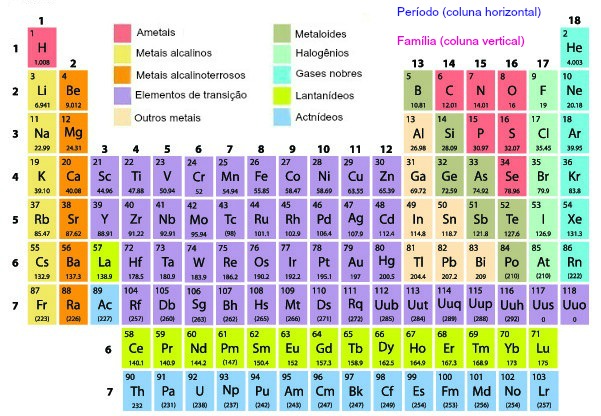
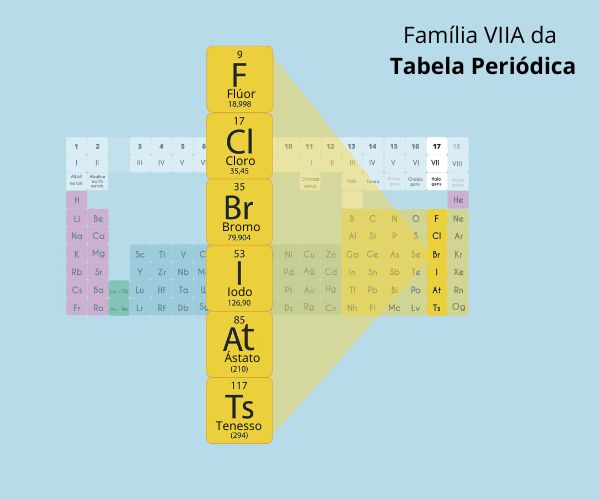
Denominamos de calcogênios todos os elementos químicos pertencentes à família VI A ou grupo 16 da Tabela Periódica. Essa família recebe esse nome pelo fato de que a grande maioria dos seus elementos forma compostos com o elemento químico cobre (Cu). Os elementos chamados calcogênios são:
-
Oxigênio (O)
-
Enxofre (S)
-
Selênio (Se)
-
Telúrio (Te)
-
Polônio (Po)
-
Un-un-hexium (Uuh)
De uma forma geral, trata-se de elementos químicos considerados ametais, ou seja, com a tendência de ganhar elétrons e formar ânions, com exceção dos elementos Polônio e Un-un-hexium, que são metálicos. Assim, os elementos dessa família podem originar compostos tanto moleculares (por meio de ligação covalente) quanto iônicos (por meio de ligação iônica).
Como estão localizados na região direita da Tabela Periódica, os calcogênios apresentam, em relação às principais propriedades periódicas, as seguintes características:
-
Possuem raio atômico pequeno quando comparados com os elementos das famílias IA a VA, por exemplo;
-
Possuem elevada energia de ionização pelo fato de apresentarem um baixo Raio Atômico;
-
Sua afinidade eletrônica e eletronegatividade são elevadas quando comparados com as outras 15 famílias à esquerda deles (IA a VA);
-
Possuem baixa eletropositividade por apresentarem baixo raio atômico.
-
São menos densos dos que os elementos localizados na região central (Família B) da Tabela Periódica.
As aplicações dos calcogênios são muito variadas. O oxigênio, por exemplo, participa de praticamente todas as reações de combustão; o selênio é utilizado na produção de xampu; o enxofre é utilizado para a produção do ácido sulfúrico; o polônio é utilizado em submarinos ou reatores nucleares, entre outras.
A principal característica dos elementos da família dos Calcogênios está no padrão que se repete na distribuição eletrônica deles. Todos eles apresentam a camada de valência com a mesma quantidade de elétrons e nos mesmos subníveis. Podemos confirmar esse fato analisando as distribuições eletrônicas desses elementos:
- Distribuição eletrônica do Oxigênio (Z = 8)
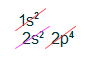
- Distribuição eletrônica do Enxofre (Z = 16)

- Distribuição eletrônica do Selênio (Z = 34)
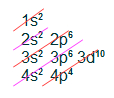
- Distribuição eletrônica do Telúrio (Z = 52)

- Distribuição eletrônica do Polônio (Z = 84)
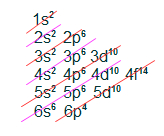
- Distribuição eletrônica do Un-un-hexiun (Z = 116)
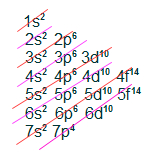
Todas as camadas de valência apresentam os subníveis s e p, bem como a mesma quantidade de elétrons, 2 e 4, respectivamente. Portanto, todos os elementos da família dos calcogênios apresentam seis elétrons na camada de valência.
Por Me. Diogo Lopes Dias