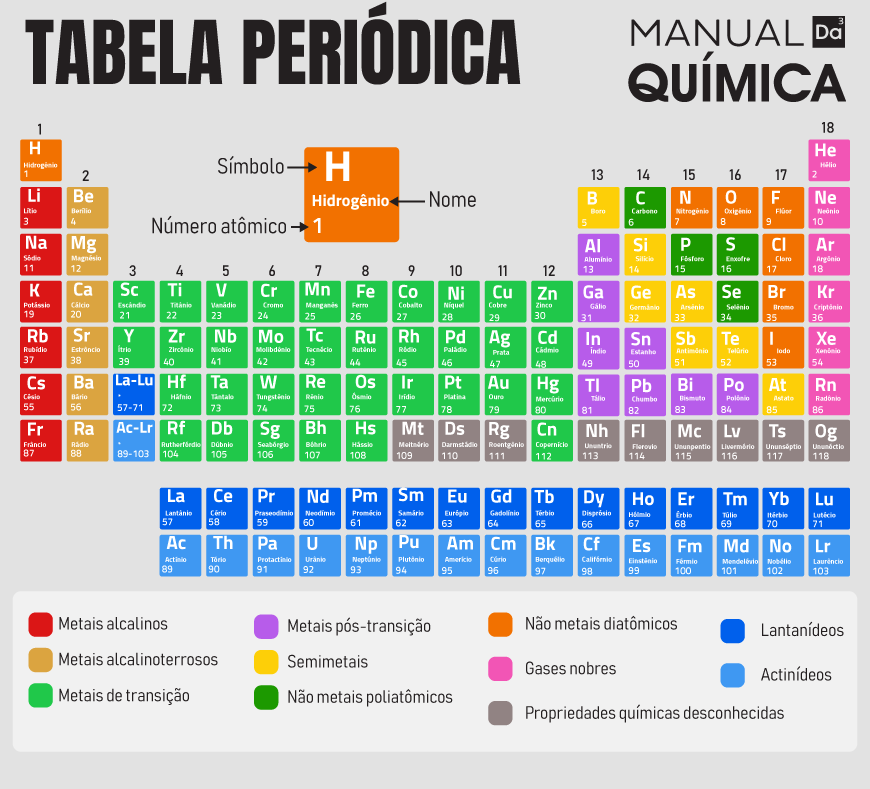
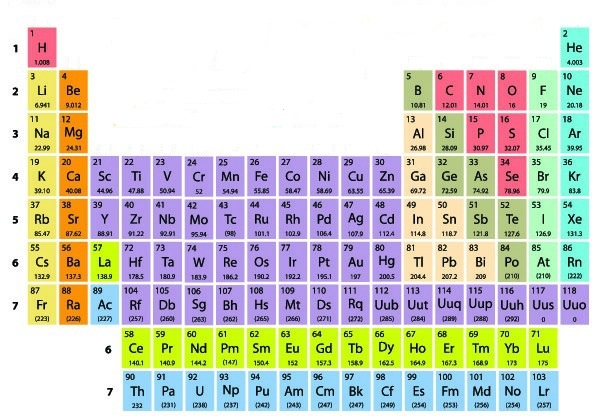
A Tabela Periódica apresenta um total de 118 elementos químicos divididos em dois grandes grupos:
-
Elementos de transição (elementos pertencentes às famílias do tipo B);
-
Elementos representativos (elementos pertencentes às famílias do tipo A).
Um detalhe interessante é que, quando abordamos especificamente os elementos de transição, temos que nos atentar para alguns elementos químicos que estão localizados do lado de fora do corpo principal da Tabela Periódica, que são os chamados elementos de transição interna.
Os elementos de transição interna da Tabela Periódica pertencem ao sexto e sétimo períodos da família IIIB. Eles estão posicionados do lado de fora por não se encaixarem de forma organizada no corpo principal da tabela.
Uma característica que se aplica aos elementos de transição interna é o fato de que todos eles apresentam como subnível mais energético o subnível f. Assim, todas as vezes que realizarmos a distribuição eletrônica de qualquer elemento de transição interna, ela terminará no subnível f. Podemos confirmar esse fato analisando as seguintes distribuições:
-
Elemento Promécio (Z = 61) – sexto período da família IIIB
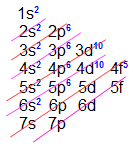
-
Elemento Plutônio (Z = 94) – sétimo período da família IIIB
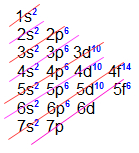
Como o diagrama de Linus Pauling apresenta o subnível f apenas duas vezes (4f e o 5f), podemos realizar algumas afirmações importantes sobre os elementos de transição interna que muitas vezes nos auxiliam e evitam até mesmo que façamos sua distribuição eletrônica.

A primeira constatação é a de que, como os elementos de transição interna estão posicionados no sexto e sétimo períodos da Tabela Periódica e temos apenas as opções 4f e 5f no diagrama, logo todos os elementos presentes no sexto período terminam sua distribuição eletrônica em 4f e os elementos do sétimo período terminam a sua distribuição em 5f.

Subnível mais energético de cada período dos elementos de transição interna
A segunda constatação é a de que, como no subnível f podemos encontrar no máximo 14 elétrons e tanto o sexto quanto o sétimo períodos que envolvem os elementos de transição interna apresentam 14 elementos, logo cada elemento apresentará uma quantidade de elétrons diferente no subnível f. Essa quantidade de elétrons sempre estará relacionada com a posição do elemento no período.
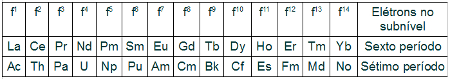
Elétrons presentes no subnível f de cada elemento de transição interna
Por Me. Diogo Lopes Dias