Podemos definir fórmula mínima ou empírica da seguinte forma:

Definição de fórmula mínima ou empírica
Por exemplo, a fórmula molecular do ácido lático é C3H9O3. Veja que a proporção entre os átomos dos elementos que compõem essa substância é de 3 : 9 : 3. Mas essa não é a proporção mínima em números inteiros, pois ela pode ainda ser simplificada pela divisão dos três números pelo menor deles (3). Assim, a proporção mínima em números inteiros dos átomos do ácido lático é de 1 : 2 : 1. Isso quer dizer que a sua fórmula mínima ou empírica é CH2O (o índice “1” não precisa ser escrito).
Veja que, nesse caso, a fórmula mínima foi diferente da fórmula molecular. Porém, observe a fórmula estrutural do etanol mostrada na figura inicial. Sua fórmula molecular é dada por C2H6O, ou seja, a proporção mínima em números inteiros dos átomos da molécula do etanol é de 2 : 6 : 1. Todavia, não é possível simplificar essa proporção ainda mais, o que nos mostra que, em alguns casos, a fórmula empírica é igual à fórmula molecular.
Outro aspecto a ser considerado é que diferentes substâncias também podem possuir a mesma fórmula mínima. Veja três compostos que possuem a fórmula mínima ou empírica igual à do ácido lático (CH2O):
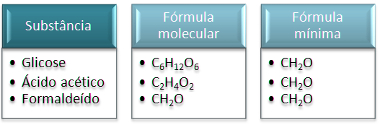
Substâncias que possuem a mesma fórmula empírica
Mas, geralmente, a fórmula mínima ou empírica não é determinada a partir da fórmula molecular. Na verdade, ocorre o contrário, ou seja, a fórmula molecular é determinada a partir da fórmula empírica. Veja como isso é feito no texto “Fórmula Molecular”.
Então, como fazemos para determinar a fórmula empírica?
* Determinação da fórmula mínima ou empírica:
Para tal, é preciso ter conhecimento sobre dois aspectos: (1) a fórmula percentual ou centesimal que indica a massa de cada elemento químico presente em 100 partes (100 g, 100 kg e assim por diante) de massa de uma substância pura e (2) as massas molares dos elementos presentes na substância.
Conhecendo a porcentagem de cada elemento na amostra, seguimos basicamente os seguintes passos:
(1) Descobrir a porcentagem em massa (em gramas): isso pode ser feito considerando-se a massa de cada elemento em exatamente 100 g do composto.
(2) Converter a porcentagem em massa (gramas) em números de mols que se encontram em exatamente 100 g do composto: divide-se a porcentagem em massa de cada elemento pela sua respectiva massa molar (dada em g/mol ou g . mol-1 - que é a mesma unidade);
(3) Conseguir os menores números inteiros: Geralmente, no passo anterior, você descobrirá as proporções entre os elementos, mas, pelo menos, algum deles não será um número inteiro, mas sim decimal. Então, para saber a proporção mínima em números inteiros, você deverá dividir o número de mols de cada elemento pelo menor número entre eles. Se ainda assim for obtido algum número decimal, você poderá multiplicar os números de mols de cada elemento por algum número inteiro positivo e pequeno, como 2 ou 3.
Vejamos dois exemplos de como determinar a fórmula mínima ou empírica das susbtâncias e como isso pode ser cobrado em exames e vestibulares:
Exemplo 1:
(UFV-MG) Sabe-se que, quando uma pessoa fuma um cigarro, pode inalar de 0,1 a 0,2 mg de nicotina. Descobriu-se em laboratório que cada miligrama de nicotina contém 74,00% de carbono; 8,65% de hidrogênio e 17,30% de nitrogênio. Calcule a fórmula mínima da nicotina. (Massas atômicas: C = 12, H = 1, N = 14).
Resolução:
(1) Descobrir a porcentagem em massa (em gramas):
Temos que C = 74,00%, H = 8,65% e N = 17,30%, o que significa que, em 100 g de nicotina, há C = 74,00 g, H = 8,65 g e N = 17,30 g.
(2) Converter a porcentagem em massa (gramas) em números de mols que se encontram em exatamente 100 g do composto. Basta dividir pelas massas atômicas:
C = 74,00 g = 6,167 mol
12 g/mol
H = 8,65 g = 8,65 mol
1 g/mol
H = 17,30 g = 1,236 mol
14 g/mol
(3) Conseguir os menores números inteiros. Basta dividir pelo menor número (1,236):
C = 6,167 = 4,9 = 5
1,236
H = 8,65 g = 6,99 = 7
1,236
N = 1,236 = 1
1,236
A fórmula mínima ou empírica da nicotina é dada por: C5H7N.
Exemplo 2:
(FEQ-CE) A análise química de uma amostra revela a seguinte relação entre os elementos químicos formadores da substância: 0,25 mol de H, 0,25 mol de S e 1,0 mol de O. Pode-se concluir que a fórmula mínima da substância é:
a) H2S2O4
b)H2SO4
c)HSO8
d)HSO4
e)HSO2
Resolução:
Nessa questão, já foram dados os valores em número de mol, por isso não precisamos seguir os passos 1 e 2, já vamos direto para o passo três:
(3) Conseguir os menores números inteiros. Basta dividir pelo menor número (0,25):
H = 0,25 = 1
0,25
S = 0,25 = 1
0,25
O = 1,0 = 4
0,25
A fórmula mínima ou empírica da substância é HSO4. A alternativa correta é a letra “d”.
Aproveite para conferir nossas videoaulas sobre o assunto: