A fórmula percentual ou centesimal, como o próprio nome diz, é aquela que indica a porcentagem (%) de cada elemento presente na substância, ou seja, a massa de cada elemento químico em 100 partes de massa da substância.
Por exemplo, se temos a fórmula percentual C75%H25%, quer dizer que em 100 gramas dessa substância há 75 g de carbono e 25 g de hidrogênio.
É possível estabelecer essa relação de proporção de massa porque isso se baseia na lei das proporções constantes vista no texto “A lei das proporções constantes de Proust”. Ela diz que as massas das substâncias que reagem em uma determinada reação e as massas das substâncias que são produzidas sempre se encontram em uma proporção fixa e constante, o que nos leva a concluir que toda substância pura contém uma proporção fixa de elementos, que é independente da massa da amostra (é uma propriedade intensiva).
Muitas vezes, nos laboratórios, os químicos não sabem qual é a composição de certa substância, por isso é necessário analisá-la por meio de algumas técnicas, como a análise de combustão, para descobrir a massa de cada elemento constituinte. Com esses valores em mão e sabendo a massa total da amostra, é fácil descobrir a fórmula percentual ou centesimal.
Isso pode ser feito de duas formas, e a primeira delas é simplesmente aplicar uma regra de três básica. Por exemplo, uma análise de uma amostra de 3,16 g de determinada substância desconhecida revelou que ela possui 2,46 g de carbono, 0,373g de hidrogênio e 0,329 g de oxigênio. Qual é a fórmula centesimal dessa substância?
Através de regras de três, temos:
|
% de C: |
% de H: |
% de O: |
Assim, a fórmula percentual dessa substância é C77,8%H11,8%O10,4%.
Outra forma de resolver essa questão seria por usar a seguinte fórmula:
Porcentagem em massa do elemento = massa do elemento na amostra . 100%
massa total da amostra
Veja que dá no mesmo:
% de C = 2,46 g . 100% % de H = 0,373g . 100% % de O = 0,329 g . 100%
3,16 g 3,16 g 3,16 g
% de C = 77,8% % de H = 11,8% % de O = 10,4%
Em muitos exercícios, podemos usar a massa molecular da substância para descobrir a porcentagem em massa do elemento. Veja um exemplo assim:
(Cesgranrio-RJ-1994) A síntese da aspirina (ácido acetilsalicílico) foi uma das maiores conquistas da indústria farmacêutica. Sua estrutura é:
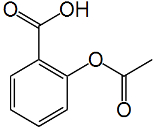
Fórmula do ácido acetilsalicílico
Qual é a porcentagem em massa de carbono na aspirina?
Dados: Massas molares: C = 12 g/mol; O = 16 g/mol; H = 1 g/mol)
a) 20 % b) 40 % c) 50 % d) 60 % e) 80 %
Resolução:
- Primeiro temos que descobrir a massa total da amostra, que, no caso, é a massa molecular. Se você tiver alguma dúvida sobre como chegar à massa molecular, leia o texto que explica esse processo.
Veja na fórmula que há 9 átomos de carbono, 8 átomos de hidrogênio e 4 átomos de oxigênio, então a fórmula molecular da aspirina é: C9H8O4:
C = (9 . 12 g/mol) = 108 g
H = ( 8 . 1 g/mol) = 8 g
O = (4. 16 g/mol) = 64 g
MM(C9H8O4) = 180 g/mol
- Agora que já sabemos a massa total, podemos usar a fórmula mostrada no texto ou regra de três para chegar ao valor da porcentagem em massa de cada elemento na amostra. O exercício pede somente a porcentagem em massa do carbono, mas faremos de todos para exemplificar:
* Por regras de três:
|
% de C: |
% de H: |
% de O: |
* Pela fórmula:
|
% de C = 108 g . 100% |
% de H = 8 g . 100% |
% de O = 64 g . 100% |
A resposta certa é a alternativa “d”.
Aproveite para conferir nossas videoaulas sobre o assunto: