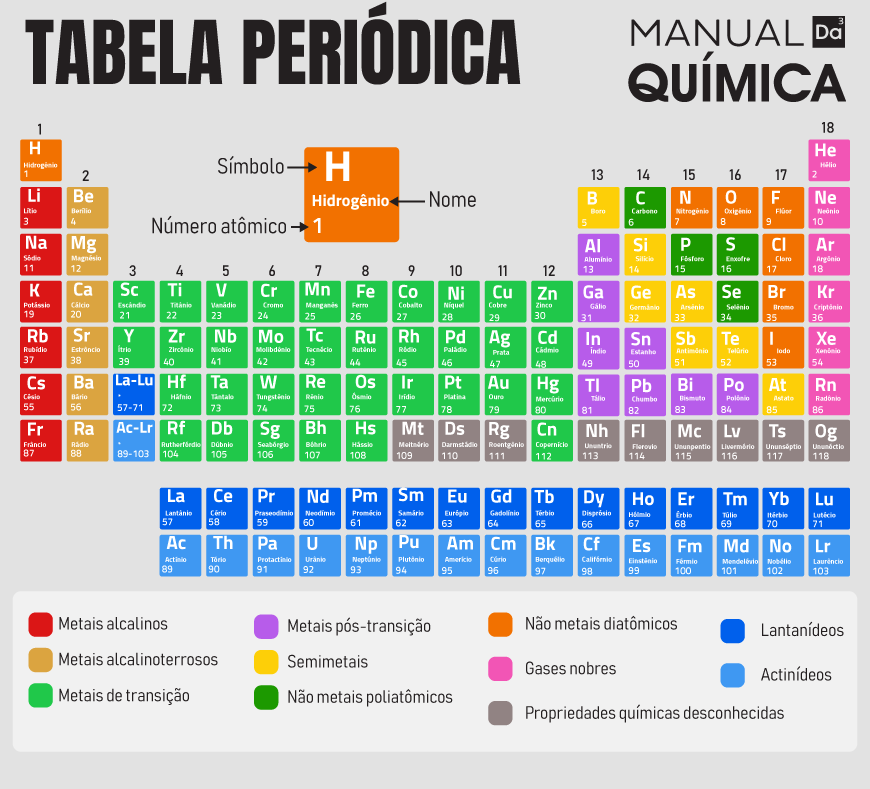
Os gases nobres são todos os elementos químicos que compõem a família VIIIA ou grupo 18 da Tabela Periódica. Os elementos que são denominados de gases nobres e seus respectivos números atômicos são:
-
Hélio-He (Z=2)
-
Neônio-Ne (Z=10)
-
Argônio-Ar (Z=18)
-
Criptônio-Kr (Z=36)
-
Xenônio-Xe (Z=54)
-
Radônio-Rn (Z=86)
Os gases nobres receberam essa denominação por dois motivos:
-
São inertes (possuem dificuldade em interagir com outros átomos);
-
São gases monoatômicos na CNTP (Condições Normais de Temperatura e Pressão). Por isso, esses gases são representados apenas pela escrita da sigla deles.
1- Inércia dos gases nobres
Como apresentam dificuldade em se combinar com outros elementos, os gases nobres são denominados de elementos estáveis e, por isso, são os elementos químicas utilizados como referência para a chamada teoria do octeto.
A teoria do octeto enuncia que um átomo de um elemento só é estável se apresentar dois ou oito elétrons na camada de valência pelo fato de que os gases nobres não interagem com outros átomos e apresentam 2 ou 8 elétrons na camada de valência (destacada em vermelho nas distribuições eletrônicas a seguir). Veja a distribuição eletrônica de cada um dos gases nobres para exemplificar a argumentação da teoria do octeto:
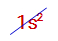
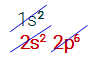

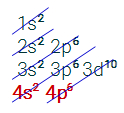


Analisando cada uma das configurações eletrônicas propostas acima, podemos observar que o Hélio apresenta dois elétrons na camada de valência, mas todos os outros cinco elementos (Neônio, Argônio, Criptônio, Xenônio e Radônio) apresentam oito elétrons. Isso confirma o fato de que, para um elemento ser estável, ele deve apresentar dois ou oito elétrons na camada de valência.
2- Ocorrência na natureza e utilização:
Os gases nobres são encontrados na natureza na forma de gases monoatômicos. O gás nobre Hélio é formado na crosta terrestre a partir de Urânio e Tório, e o gás nobre Radônio é originado na crosta terrestre a partir de Rádio e Tório, sempre por meio do processo de decaimento radioativo.
Os gases nobres apresentam as seguintes características:
-
Baixos pontos de fusão e ebulição;
-
Elevada energia de ionização;
-
Baixa reatividade;
-
Difundem-se facilmente por meio do vidro e da borracha.
A utilização desses gases monoatômicos pelo ser humano engloba diversos ramos de atividades, a saber:
-
Hélio: cilindro utilizado por mergulhadores e em balões e dirigíveis;
-
Neônio: Utilizado em válvulas estabilizadoras de tensão e anúncios luminosos;
-
Argônio: Utilizado em atmosferas inertes para realização de fusão de materiais; utilizado também na solda de metais;
-
Criptônio: Ainda não é utilizado em nenhuma atividade humana importante;
-
Xenônio: Utilizado em iluminação pública e na produção de flashes eletrônicos;
-
Radônio: É utilizado para a determinação da idade geológica de algumas rochas.
Por Me. Diogo Lopes Dias