Os átomos, elétrons, moléculas e íons são entidades muito pequenas, invisíveis aos olhos humanos. Quando se fala, por exemplo, da massa atômica de um elemento, não se trata de uma quantidade que possa ser trabalhada pelos cientistas, pois, uma unidade de massa atômica corresponde a doze avos (1/12) da massa de um átomo de carbono-12. Temos, por exemplo, que a massa atômica de 1 átomo de hidrogênio é 1 u, a do oxigênio é 16 u e da molécula de água (H2O) é 18 u (2 . 1 + 16).
Portanto, os químicos precisavam de uma quantidade que fosse mensurável, que pudesse ser “pesada” em gramas. Por isso, eles começaram a adotar “porções” de átomos. Eles queriam uma quantidade de átomos que representasse em gramas o mesmo valor da massa atômica. Por exemplo, como mostra o esquema abaixo, 1 átomo de cálcio tem massa atômica de 40 u. Então, para o cálcio, a grandeza que se buscava deveria ter uma quantidade de átomos que, sendo “pesada”, fornecesse 40 gramas:
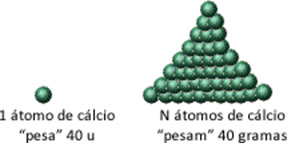
Relação entre massa atômica do cálcio e grandeza que se buscava
Foi aí que surgiu o conceito de “mol”, palavra criada em 1896 pelo químico alemão Wilhelm Ostwald (1853-1932). Essa palavra vem do latim moles, que significa “porção”, “monte”, “amontoado” ou “quantidade”.
O mol é uma das sete grandezas de base do Sistema Internacional de Unidades (SI) e é denominada de quantidade de matéria. Ele pode ser conceituado da seguinte maneira:
“Mol é a quantidade de matéria de um sistema que contém tantas entidades elementares quantos são os átomos contidos em 12 gramas de carbono-12.”
Isso significa que 1 mol de C-12 tem 12 g, da mesma forma que 1 mol de Ca tem 40 g, que 1 mol de H tem 1g, que 1 mol de O tem 16 g e que 1 mol de água tem 18 g.
A palavra “mol” pode criar algumas confusões, pois ela é usada tanto para se referir ao nome da unidade como para se referir ao símbolo dela. Por exemplo, a título de comparação, temos que a grandeza de comprimento possui como unidade o metro, que é simbolizado por “m”. Assim, quando falamos o nome “metro”, ele pode aparecer no plural, mas quando nos referimos ao símbolo “m”, ele não vai para o plural, como se pode ver nos dois exemplos a seguir:
-
“O comprimento dessa caixa é 2 metros.” → nome no plural;
-
“O comprimento dessa caixa é 2 m.” → símbolo não vai para o plural.
O mesmo vale para o mol. Se estivermos nos referindo ao nome da unidade, podemos falar o plural “mols”, como em “Quantos mols correspondem a 88 g de CO2?”; mas se for o símbolo da unidade, isso não pode acontecer, como em “88 g de CO2 têm 2 mol.”.
Assim, quando nos referimos à massa de 1 mol de qualquer substância, elemento, átomo, íon, etc., estamos nos referindo à massa molar, simbolizada por “M” e cuja unidade é gramas por mol (g/mol). Por exemplo, a massa molar do cálcio é 40 g/mol e a da água é 18 g/mol.
Então, temos que o valor da massa molar será o mesmo dado para a massa atômica, mudando somente a unidade, que de “u” vai para “g/mol”.
O número de mol ou quantidade de matéria também pode ser simbolizado pela letra “n”. Para calcular quantos mols existem em uma determinada massa de um elemento químico ou de uma substância, basta usarmos regras de três ou a seguinte fórmula matemática:
n = m
M
Sendo que:
n = quantidade de matéria (em mol);
m = massa dada (em gramas);
M = massa molar (em g/mol)
Mas surge outra questão: Quantas entidades (partículas, átomos, moléculas, elétrons ou íons) tem 1 mol de qualquer substância?
Isso é atualmente determinado por vários métodos experimentais, tais como eletrólise, emissões radioativas, raios X, entre outras, e todas apontam para valores muito próximos à constante de Avogadro, cujo valor é 6,02 . 1023. Portanto, temos que 1 mol sempre contém 6,02 . 1023 entidades. Veja os exemplos abaixo:
-
1 mol de H2O possui 6,02 . 1023 moléculas;
-
1 mol de Ca possui 6,02 . 1023 átomos;
-
1 mol de O2- possui 6,02 . 1023 íons;
-
1 mol de NaCl possui 6,02 . 1023 fórmulas.
Aproveite para conferir nossas videoaulas sobre ao assunto: