O termo “metal” (palavra oriunda do grego metalon) refere-se a uma das quatro classificações propostas para os elementos químicos da Tabela Periódica (sendo as outras: ametais, gases nobres e hidrogênio). São metais 94 dos 118 elementos existentes na Tabela.
Dos 94 metais existentes, 68 são denominados de metais de transição por pertencerem às famílias B. Desses 68, 40 são metais de transição externa (por apresentarem o subnível d como mais energético, como a Prata) e 28 são de transição interna (por apresentarem o subnível f como mais energético, como o Európio).

Distribuição eletrônica do metal prata
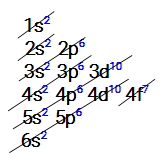
Distribuição eletrônica do metal európio
Os outros 26 metais são os elementos representativos, pois apresentam o subnível s (como o cálcio) ou p (como o alumínio) como subnível mais energético.
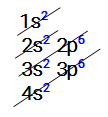
Distribuição eletrônica do metal cálcio
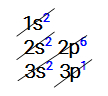
Distribuição eletrônica do metal alumínio
Características físicas dos metais
-
São sólidos em temperatura ambiente, com exceção do mercúrio, que é líquido;
-
Apresentam coloração prateada, com exceção do ouro (amarelado) e do cobre (avermelhado);
-
Apresentam brilho;
-
Apresentam elevados pontos de fusão e ebulição, com exceção do mercúrio (Ponto de fusão: 38,83oC; Ponto de Ebulição: 356,7oC);
-
São dúcteis (podem ser transformados em fios);
-
São maleáveis (podem ser transformados em lâminas);
-
Os metais apresentam baixíssima elasticidade, tendo, então, uma alta resistência à tração;
-
São condutores de calor,
-
São condutores de corrente elétrica;
-
Possuem elevada tenacidade (resistência mecânica);
-
Possuem baixa dureza (capacidade de riscar), com exceção dos metais irídio e crômio;
-
Apresentam elevada eletropositividade (capacidade de perder elétrons e transformar-se em cátion).
Ligações químicas envolvendo os metais
Os átomos de um metal estão ligados entre si por meio da chamada ligação metálica. Nela os átomos de um metal perdem elétrons (formando cátions do metal) e esses elétrons fazem com que os átomos do metal agrupem-se, formando uma estrutura cristalina cercada por um ''mar de elétrons''.
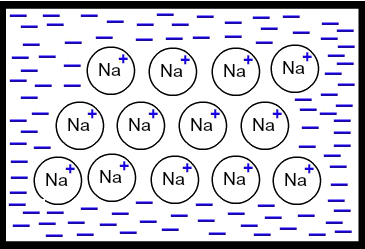
Desenho ilustrando o modelo do mar de elétrons
Quando o átomo de um metal estabelece ligação química com um elemento que não apresenta característica metálica, origina um composto iônico, o qual é formado a partir de ligação iônica.
OBS.: Existem alguns casos raros em que, quando um metal interage com um ametal ou hidrogênio, há o compartilhamento de elétrons (ligação covalente) entre esses átomos. O berílio é um metal que estabelece ligações covalentes quando interage com ametal ou hidrogênio, como no caso da substância BeH2.
Características químicas dos metais
Os metais participam da formação de diversos grupos de substâncias, como:
-
Peróxidos
Eles também realizam reações de simples troca com outras substâncias. Nessas reações, o metal (Me) troca de posição com o metal (X) ou com o hidrogênio (H) presente na substância composta utilizada:
Me + XY → MeY + X
ou
Me + HY → MeY + H2
Para que a reação de simples troca aconteça, o metal utilizado deve ser mais reativo que o hidrogênio ou que o metal presente na substância composta. Veja a fila decrescente de reatividade a seguir:
Li>Rb>K>Cs>Ba>Sr>Ca>Na>Mg>La>Zn>Cr>Fe>Cd>Co>Ni>Sn>Pb>H>Cu>Hg>Ag>Pd>Pt>Au
Exemplo 1: Reação entre um metal e um ácido
Quando um metal reage com um ácido, o metal pode deslocar o hidrogênio presente na substância, liberando gás hidrogênio (H2) e formando um sal inorgânico, como no exemplo a seguir:
2 Al + 6 HCl → 2 AlCl3 + 3 H2
Exemplo 2: Reação entre um metal e um sal qualquer
Quando um metal reage com um sal que apresenta um metal menos reativo que ele, ocorrerá a troca de posição entre o metal reagente e o metal presente no sal. Assim, haverá a formação de um novo sal e de um novo metal isolado, como no exemplo a seguir:
Zn + CuCl2 → ZnCl2 + Cu
Exemplo 3: Reação entre um metal e água
De uma forma geral, quando um metal reage com água, temos a formação de uma base inorgânica e gás hidrogênio, como no exemplo a seguir:
Na + H2O → NaOH + ½ H2
Formas de obtenção dos metais
De forma geral, os metais são obtidos a partir de rochas minerais e estão associados a outros materiais ou elementos. Assim sendo, é necessário separá-los, o que ocorre por meio de técnicas da siderurgia, como a eletrólise, ou ainda por meio de reação química com outras substâncias. Veja alguns nomes de minerais e os metais que podem ser extraídos a partir deles:
-
Hematita: Dela é obtido o ferro
-
Cassiterita: Dela é obtido o estanho
-
Galena: Dela é obtido o chumbo
-
Esfarelita: Dela é obtido o zinco
OBS.: Alguns metais podem ser encontrados de forma isolada na natureza, já que eles apresentam dificuldade de se associar com outros elementos, como é o caso do ouro, platina, paládio, cobre e prata.
Por Me. Diogo Lopes Dias