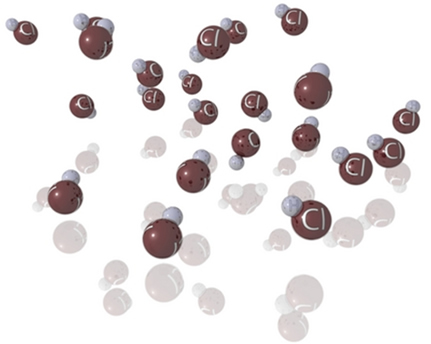
Conforme explanado no texto Estados Físicos da Matéria, os três estados físicos ou de agregação básicos da matéria são sólido, líquido e gasoso. Eles diferenciam-se exatamente pela organização das suas partículas constituintes, ou seja, por sua agregação, se estão próximas ou afastadas umas das outras.
No estado sólido, as partículas encontram-se mais juntas; no estado líquido, possuem maior liberdade de movimentação; e, no estado gasoso, estão bem afastadas umas das outras. Todas as substâncias podem ser encontradas nesses três estados físicos, a depender apenas de duas grandezas: a temperatura e a pressão. Alterando essas duas grandezas, podemos mudar o estado de agregação das substâncias.
A temperatura e a pressão atuam de formas contrárias, enquanto o aumento da temperatura faz com que as moléculas afastem-se, o aumento da pressão faz com que elas fiquem mais próximas umas das outras.
Um exemplo é a solubilidade do gás dióxido de carbono usado nos refrigerantes. No momento da fabricação, uma pressão muito grande e temperaturas baixas são aplicadas para que o gás passe para o estado líquido, solubilizando-se. Quando abrimos a tampa do refrigerante, o gás sai mais rapidamente porque diminuímos a pressão. Além disso, quanto maior estiver a temperatura, também maior será a velocidade de saída do gás.
Mas considerando a pressão atmosférica normal, que é ao nível do mar e igual a 1 atm ou 760 mmHg, para mudarmos os estados físicos das substâncias, é preciso haver apenas um aumento ou diminuição da temperatura.
Considere um cubo de gelo a -20 ºC sob pressão de 1 atm, por exemplo. As suas moléculas estão bem unidas e é por isso que sua estrutura é rígida, apresentando volume e formato definidos. Mas se quisermos passar esse gelo para o estado líquido, é necessário que suas moléculas separem-se mais. Para tal, é preciso introduzir energia ao sistema, de modo que ela possa “vencer” as forças intermoleculares existentes entre as moléculas de água, que estão unidas por ligações de hidrogênio, que são bastante intensas.

Estrutura das moléculas de gelo
Se aquecermos o sistema, a temperatura aumentará gradativamente até atingir o ponto de fusão ou temperatura de fusão. A palavra fusão corresponde à mudança do estado sólido para o líquido, que, no caso da água, ocorre em 0ºC ao nível do mar. Nesse momento, a temperatura permanecerá constante até que todo o gelo passe para o estado líquido, ou seja, vão coexistir os estados sólido e líquido.

Moléculas de água no estado líquido
Quando tudo tiver passado para o estado líquido, a temperatura continuará aumentando e as moléculas separar-se-ão cada vez mais até atingir o ponto de ebulição. A ebulição é a passagem do estado líquido para o gasoso (ou vapor, no caso da água), de modo uniforme, quando se aumenta a temperatura. Mas existem ainda mais outras duas formas de passagem do estado líquido para o gasoso, que são a evaporação e a calefação. Veja a seguir a diferença entre as mudanças de estado chamadas de vaporização, evaporação, ebulição e calefação:
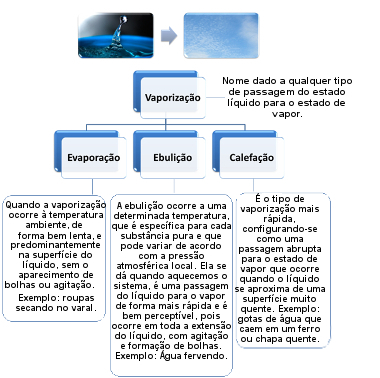
Tipos de vaporização: evaporação, ebulição e calefação
O ponto de ebulição da água ao nível do mar é 100ºC, e a temperatura permanece constante até que todo o líquido passe para o estado de vapor. Posteriormente, a temperatura do vapor continuará subindo, indo para 101ºC, 102ºC, 103ºC e assim sucessivamente.
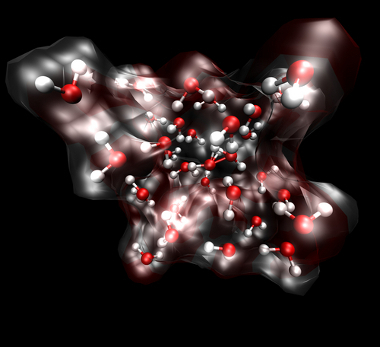
Moléculas de água no estado de vapor
O processo inverso ocorre pela diminuição da temperatura do sistema. Quando diminuímos a temperatura, o vapor de água, quando atinge 100ºC, começa a passar para o estado líquido. Essa mudança de estado é chamada de liquefação ou condensação. É o que ocorre, por exemplo, quando as nuvens condensam-se e formam a chuva.
Diminuindo ainda mais a temperatura do líquido, ele atinge 0ºC e começa a passar para o estado sólido. Essa mudança do estado líquido para o sólido é denominada solidificação.
Existe ainda outra mudança de estado físico, que é a sublimação. Ela ocorre quando a substância passa diretamente do estado sólido para o estado gasoso ou vice-versa. Esse fenômeno ocorre com o gelo-seco e com a naftalina, por exemplo.
Resumidamente, temos as seguintes cinco mudanças de estado físico:
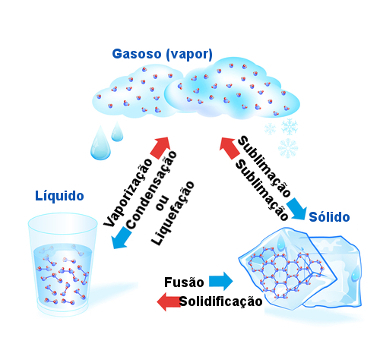
Esquema de mudanças de estados físicos
Aproveite para conferir nossas videoaulas relacionadas ao assunto: