As propriedades das substâncias são influenciadas em grande parte pelo tipo de ligação que seus átomos realizam e se elas são polares ou apolares. Por exemplo, o álcool (etanol), H3C — CH2 — OH, possui a propriedade de ser infinitamente solúvel em água e, ao mesmo tempo, ser solúvel na gasolina, sendo que ambas não se misturam. Isso ocorre porque a água é polar e o etanol também possui ligações polares em suas moléculas, mas, por outro lado, a gasolina é apolar, sendo que o etanol também possui ligações apolares em suas moléculas.
Antes de verificarmos quais são as ligações apolares e as polares das moléculas do etanol, vejamos como determinar a polaridade das ligações iônicas e covalentes:
1. Ligações iônicas:
As ligações iônicas são aquelas em que os átomos dos elementos transferem um ou mais elétrons definitivamente um para o outro, formando íons. O átomo do elemento que perdeu os elétrons é o cátion (fica com carga positiva) e o átomo do elemento que recebeu os elétrons é o ânion (fica com carga negativa).
Assim, toda ligação iônica ocorre com diferença de eletronegatividade entre os átomos envolvidos, visto que sempre envolve partículas de cargas opostas, formando-se polos, um negativo e um positivo. Portanto, podemos concluir que:
Toda ligação iônica é polar.
2. Ligações covalentes:
As ligações covalentes são aquelas em que ocorre compartilhamento de pares de elétrons entre os átomos. Assim, dependendo do tipo de elemento que está envolvido na ligação, ela pode ser polar ou apolar. O etanol realiza somente ligações covalentes, de modo que em sua molécula ocorre os dois tipos de ligações (ligação covalente apolar e ligação covalente polar).
Veja:
2.1. Ligação covalente apolar:
Quando a ligação ocorre entre dois átomos de um mesmo elemento químico, não há diferença de eletronegatividade entre eles e, por isso, a distribuição dos elétrons ao redor do núcleo de ambos os átomos é simétrica e não há formação de polos carregados positivamente ou negativamente na molécula.
Por exemplo, a molécula de etanol (H3C — CH2 — OH) possui uma ligação covalente entre dois átomos de carbono, sendo uma ligação apolar, como é mostrado abaixo. Além disso, a diferença de eletronegatividade entre o carbono e o hidrogênio é mínima, por isso a região H3C — CH2 da molécula do etanol é considerada apolar e é responsável pela sua propriedade de ser solúvel na gasolina.
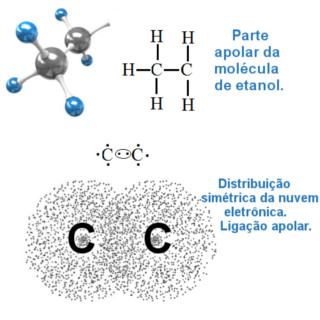
Ligação covalente apolar entre átomos de carbono do etanol
2.2. Ligação covalente polar:
Quando a ligação covalente ocorre entre átomos de elementos que possuem diferentes eletronegatividades, um dos átomos – o mais eletronegativo – atrai com maior força os elétrons da ligação, criando uma diferença de distribuição da nuvem eletrônica. Com isso, forma-se uma região com maior densidade de elétrons, que fica com carga parcial negativa (δ-), e uma região com menor densidade de elétrons, que fica com carga parcial positiva (δ+). Visto que há compartilhamento de elétrons e não transferência, no caso das ligações covalentes, não se pode representar o polo negativo pelo sinal - e nem o polo positivo pelo sinal +. Isso é feito somente nas ligações iônicas que são constituídas de íons. Por isso, aqui usamos “carga parcial”, simbolizada por “δ”.
Um dos elementos mais eletronegativos é o oxigênio. Por isso, as ligações que ele realiza com o carbono e com o hidrogênio são polares, tendo em vista que ele atrai mais fortemente os elétrons da ligação. O oxigênio fica com carga parcial negativa (δ-), enquanto o carbono e o hidrogênio ficam com carga parcial positiva (δ+):
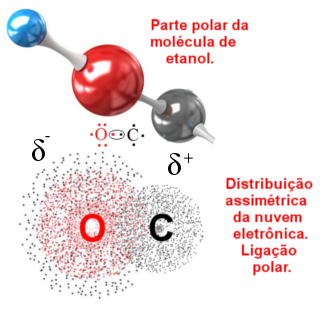
Ligação covalente polar entre átomos de carbono e oxigênio
Quanto maior for a diferença de eletronegatividade entre os elementos da ligação, maior será a polaridade da ligação. O cientista Linus Pauling criou uma escala de eletronegatividade para os elementos da Tabela Periódica, sendo que, considerando os elementos principais, temos:
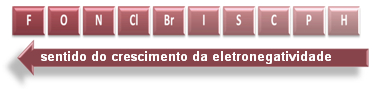
Escala de eletronegatividade de Pauling
Isso significa que a ligação do fluoreto de hidrogênio (H— F) é a mais eletronegativa. Existe uma frase que nos ajuda a lembrar tal escala de eletronegatividade. Veja abaixo que as iniciais das palavras correspondem ao símbolo de cada elemento da escala:
“Fui Ontem No Clube, Briguei I Sai Correndo Para o Hospital.”
Assim, sobre os tipos de ligações covalentes, resumindo, temos:
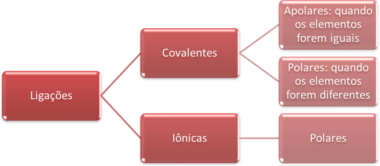
Resumo da polaridade das ligações
Aproveite para conferir as nossas videoaulas relacionadas ao assunto: