Entre todos os elementos químicos que conhecemos, somente os gases nobres, elementos pertencentes à família 18 (ou VIII A) da tabela periódica, aparecem na natureza na forma isolada. Todos os demais são encontrados na natureza somente formando substâncias simples ou compostas, ou seja, os átomos ligam-se a outros átomos.
Essas ligações químicas tornam o átomo mais estável do que no seu estado fundamental, pois ele perde energia no momento que realiza a ligação. É por essa estabilidade que é possível que substâncias ao nosso redor durem tanto tempo, como é o caso das presentes nos ossos dos dinossauros, que duram milhões de anos.
O químico Walther Kossel (1888-1956) analisou essa relação entre a estabilidade dos gases nobres e a sua configuração eletrônica e criou, em 1916, a teoria eletrônica de valência. Valência corresponde ao número de ligações que cada átomo deve fazer para ficar estável. Por exemplo, o carbono é tetravalente, o que significa que ele precisa realizar quatro ligações químicas para ficar estável. Além disso, a camada mais externa ao núcleo, que é onde ocorrem as ligações químicas, é chamada de camada de valência.
Os gases nobres possuem exatamente oito elétrons na sua camada de valência (com exceção do hélio que possui somente dois elétrons, porque o seu nível mais externo é o primeiro). Veja:

Distribuição eletrônica em ordem geométrica dos gases nobres
Assim, Kossel relacionou a estabilidade desses elementos com essa configuração eletrônica. Portanto, para os demais elementos químicos ficarem estáveis, eles teriam que ter a mesma configuração eletrônica dos gases nobres.
Essa ideia foi aperfeiçoada com o tempo por Gilbert Newton Lewis (1875-1946) e Irving Langmui (1881-1957). Esse último chamou-a de regra do octeto ou teoria do octeto, que basicamente diz o seguinte:
“Um grande número de átomos adquire estabilidade quando possui 8 elétrons na camada de valência, ou 2 elétrons quando possui somente a primeira camada.”
Assim, para adquirir essa estabilidade eletrônica, os átomos de diferentes elementos estabelecem ligações entre si, doando, recebendo ou compartilhando elétrons, de modo que todos os átomos adquiram a configuração de um gás nobre correspondente (com o mesmo número de camadas eletrônicas.
Por exemplo, os elementos da família 1 possuem todos apenas um elétron na camada de valência. Dessa forma, eles possuem a tendência de perder esse elétron para que sua camada de valência seja a anterior, que já possui oito elétrons. O hidrogênio e o lítio são exceções, pois o hidrogênio precisa ganhar mais um elétron e o lítio precisa perder um elétron para que ambos fiquem com dois elétrons na camada K.
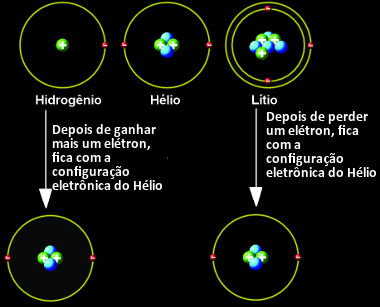
Hidrogênio e lítio ficam estáveis com a configuração do hélio (gás nobre)
Veja outro exemplo para entender melhor: os elementos da família 16 possuem seis elétrons na camada de valência, por isso eles precisam receber dois elétrons para ficarem estáveis.
A seguir, temos as regras gerais para a maioria dos elementos das famílias representativas:
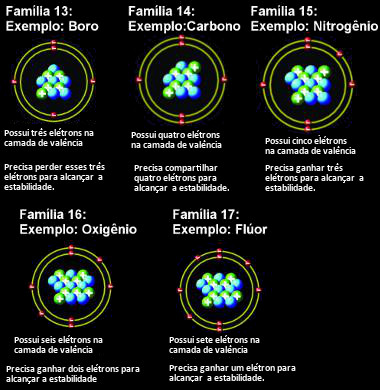
O que deve acontecer com os átomos de cada família para ficarem estáveis segundo a teoria do octeto
Para ver exemplos de como isso ocorre, leia os textos Ligação Iônica e Ligação Covalente.
Por Jennifer Fogaça
Graduada em Química
Videoaulas relacionadas: