Os materiais que usamos no cotidiano, os medicamentos que tomamos para combater doenças, os alimentos industrializados, entre outros produtos que não vivemos sem, são resultado de reações orgânicas em que os químicos sabem combinar de maneira correta os reagentes a fim de obter o item desejado.
Visto que existem milhões de substâncias orgânicas, a quantidade de reações possíveis entre elas também é muito grande. Porém, elas seguem padrões bem definidos e podem ser mais facilmente previstas.
Desse modo, as principais reações orgânicas feitas em laboratórios e indústrias foram classificadas como sendo as reações de substituição, de adição e de eliminação. Neste texto será explicado sobre as reações de substituição:

Definição de reações de substituição
Genericamente, temos que uma reação de substituição pode ser representada da seguinte forma:
| |
– C – A + BX → – C – B + AX
| |
As reações de substituição ocorrem especialmente com alcanos, hidrocarbonetos aromáticos (benzeno e seus derivados) e com haletos orgânicos.
Visto que essas reações são moleculares, elas são mais difíceis de ocorrer e mais lentas, pois deve haver a quebra de uma ligação entre o átomo que será substituído e o carbono da cadeia, além da formação de uma nova ligação com o radical substituinte. Assim, essas reações ocorrem em condições energéticas, envolvendo altas temperaturas, altas pressões, uso de catalisadores e de luz.
Veja os cinco principais exemplos de reações de substituição:
-
Halogenação: É assim chamada porque ocorre com as substâncias simples dos halogênios: F2, Cl2, Br2 e I2. No entanto, as mais comuns são a cloração (Cl2) e a bromação (Br2).
Exemplo: Monocloração do etano: O hidrogênio é substituído pelo cloro.
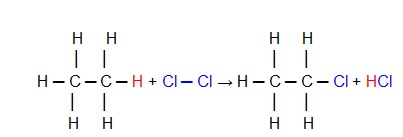
Quando a molécula do alcano é mais complexa e existem várias possibilidades de substituições, será obtida uma mistura de diferentes compostos orgânicos. Como no caso abaixo:
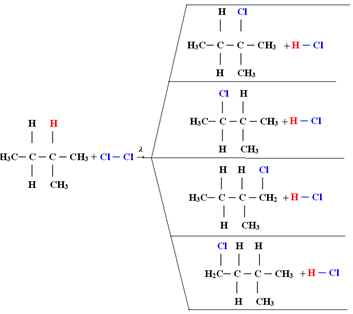
Reação de monocloração do metilbutano
A porcentagem desses produtos é influenciada em grande parte pela ordem de facilidade com que o hidrogênio “sai” do hidrocarboneto. Hidrogênios ligados a carbonos terciários saem com maior facilidade, seguidos dos ligados aos carbonos secundários e, por fim, os primários.
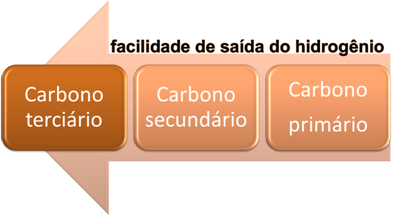
Ordem de facilidade de saída do hidrogênio em reações de substituição em alcanos
-
Nitração: Ocorre com o ácido nítrico.
Exemplo: Nitração do metano:
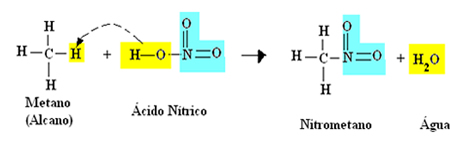
Reação de nitração com a formação de nitrometano
-
Sulfonação: Ocorre com o ácido sulfúrico.
Exemplo: Sulfonação do benzeno:
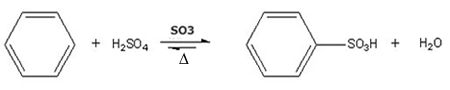
Reação de sulfonação do benzeno
-
Alquilação: É conhecida por Alquilação de Friedel-Crafts porque foi concluída pela primeira vez por esses dois cientistas em 1877. Esse tipo de reação ocorre com os aromáticos e com os haletos orgânicos, em que pelo menos um de seus hidrogênios é substituído por um radical alquila.
Pode ser usado o cloreto de alumínio anidro como catalisador ou outros catalisadores, como o FeCl3.
Exemplo: Metilação do benzeno:
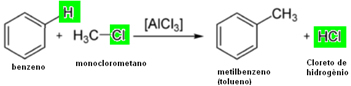
Reação de alquilação – metilação do benzeno
-
Acilação: Essa reação ocorre quando um hidrogênio do anel aromático é substituído por um grupo acila, mostrado abaixo:
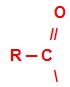
Exemplo: Acilação do benzeno:
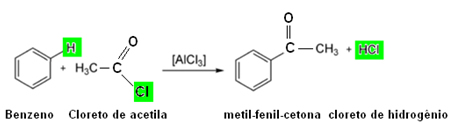
Reação de acilação do benzeno
-
Hidrólise alcalina: Essa reação ocorre com os haletos orgânicos quando sofrem quebra na presença de uma solução aquosa de base forte e álcoois são formados como produtos.
Exemplo: hidrólise alcalina do cloreto de etila (cloroetano) em que é formado o etanol:
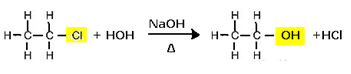
Reação de substituição (hidrólise alcalina) do cloroetano para a formação de um álcool
Por Jennifer Fogaça
Graduada em Química