Sais de ácidos carboxílicos são substâncias orgânicas oxigenadas, formadas a partir da reação de neutralização entre um ácido carboxílico e uma base inorgânica qualquer, como podemos observar na equação abaixo:
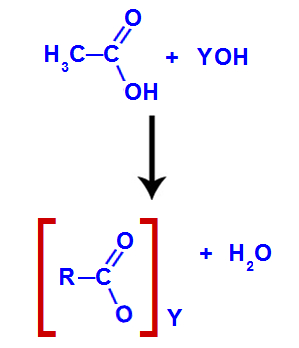
Equação de neutralização entre um ácido carboxílico e uma base
Nessa reação, o grupo hidróxido (OH-) da base interage com o cátion hidrônio (H+) presente no grupo OH do ácido carboxílico, formando a molécula de água. Já o sal de ácido carboxílico é formado quando o cátion da base interage com o oxigênio do ácido que perdeu o hidrônio.
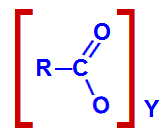
Fórmula estrutural de um sal de ácido carboxílico qualquer
Características
a) Estado físico
À temperatura ambiente, os sais de ácido carboxílico são sólidos, de estrutura cristalina.
b) Solubilidade
Os sais de ácidos carboxílicos formados por metais alcalinos (família IA da tabela periódica) ou com amônio (cátion de fórmula NH4+) apresentam boa solubilidade em água. Os sais com qualquer outro cátion são praticamente insolúveis, principalmente os de metais pesados.
c) Densidade
São substâncias com uma densidade maior que a da água.
d) Forças intermoleculares
São moléculas de características polares mistas, já que sua parte formada por carbonos e hidrogênios apresenta um caráter apolar, e a extremidade que possui ligação iônica apresenta caráter polar.
e) Ponto de fusão e de ebulição
Tanto a temperatura de fusão quanto a de ebulição é bastante elevada, assim, em vez de sofrer mudança de estado físico, é mais fácil a molécula sofrer uma decomposição.
f) Propriedades organolépticas (que estimulam os sentidos)
Os sais de ácidos carboxílicos são inodoros (não estimulam o olfato) e adstringentes, mesmo sendo sais.
Nomenclatura oficial pela União Internacional de Química Pura e Aplicada (IUPAC)
Prefixo do número de carbonos + infixo + oato + de + nome do cátion
Exemplo 1: Sal de ácido carboxílico com cátion não metálico.
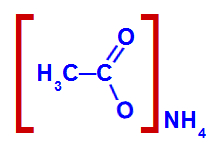
Estrutura do sal de ácido carboxílico com cátion não metálico
A cadeia desse sal de ácido carboxílico apresenta:
- Quatro átomos de carbono (prefixo but);
- Apenas ligações simples entre os carbonos (infixo an);
- Sufixo oato (por ser um sal de ácido);
- Preposição de (por ser um sal);
- O cátion não metálico amônio (NH4+).
Assim, o nome desse sal de ácido carboxílico é etanoato de amônio.
Exemplo 2: Sal de ácido carboxílico com cátion metálico.
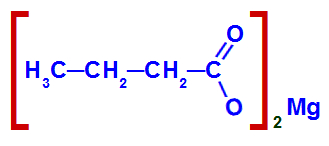
Estrutura do sal de ácido carboxílico com cátion metálico
A cadeia desse sal de ácido carboxílico apresenta:
- Dois átomos de carbono (prefixo et);
- Apenas ligações simples entre os carbonos (infixo an);
- Sufixo oato (por ser um sal de ácido);
- Preposição de (por ser um sal);
- O metal magnésio (Mg).
Assim, o nome desse sal de ácido carboxílico é butanoato de magnésio.
Utilizações
Os sais de ácidos carboxílicos apresentam, de uma forma geral, como principal utilização a formação de sabões, ou seja, são usados em indústrias de fabricação de sabões (produto cuja ação básica é limpar).
Isso ocorre porque a ação de limpeza é determinada por moléculas que apresentam uma parte polar (por apresentarem ligação iônica em uma extremidade) e uma parte apolar (por apresentar uma sequência de carbonos e hidrogênios), como é o caso dos sais de ácidos carboxílicos.